Taiana G. M. Bonadio e Wilson R. Weinand
A pesquisa e desenvolvimento de biomateriais vêm sendo estimulada por avanços em biologia celular e molecular, química, ciência de materiais e engenharias. A comunidade biomateriais tem sido a principal contribuinte para a compreensão das interações dos materiais com o ambiente fisiológico. O desenvolvimento de biomateriais para aplicações na área da saúde tem evoluído através de três gerações, cada uma com um objetivo diferente conforme ilustrado na Figura 1.
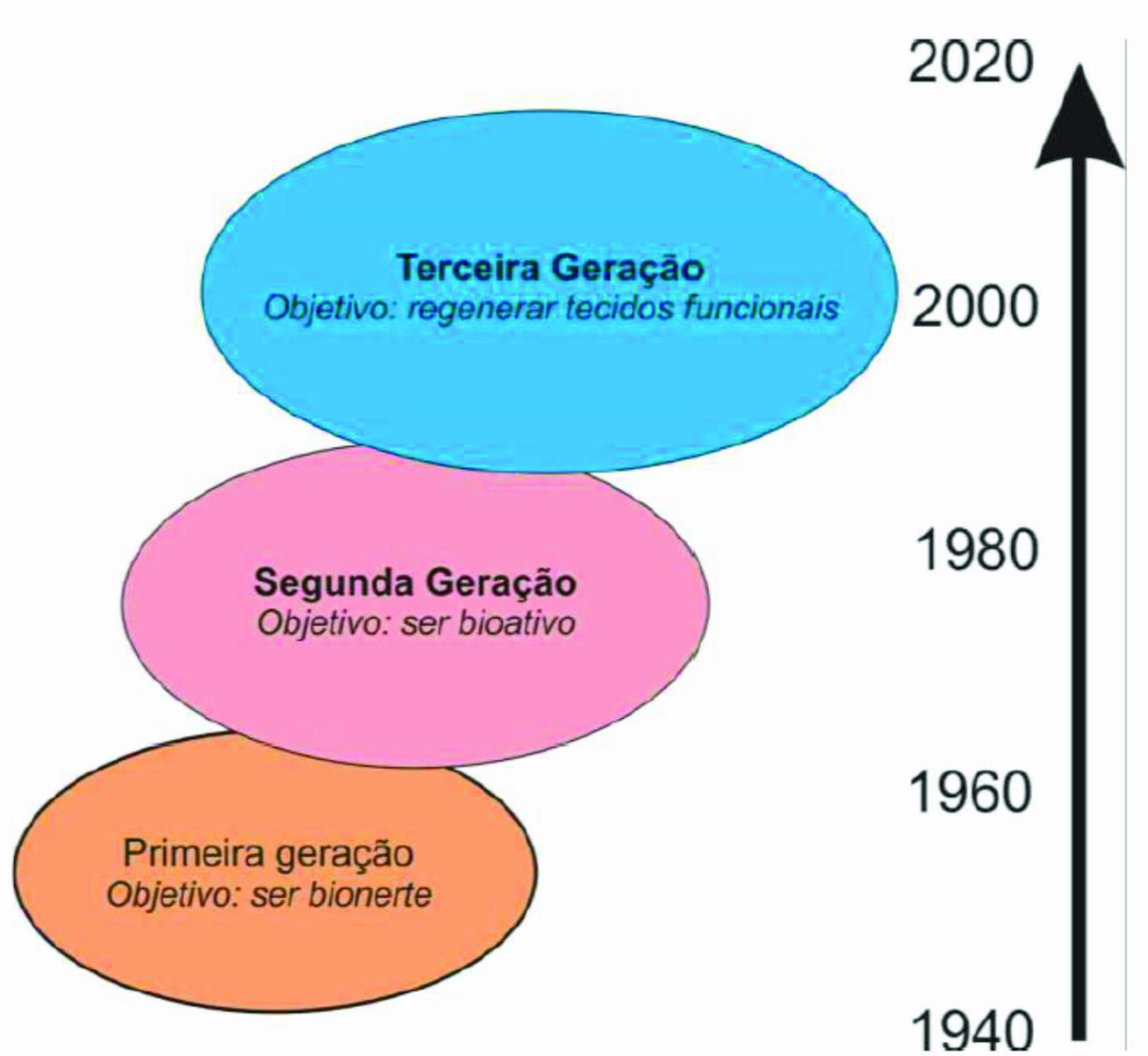
Figura 1. Evolução da ciência e tecnologia em biomateriais.
O objetivo dos primeiros biomateriais (primeira geração) foi alcançar uma combinação adequada entre suas propriedades funcionais com as do tecido substituído sem uma resposta prejudicial por parte do hospedeiro. Assim, como os materiais desenvolvidos durante a guerra, os biomateriais de primeira geração (a partir de 1950 e 1960) foram em grande parte compostos de materiais industriais conhecidos como off-the-shelf (fora da prateleira). Isto é, materiais amplamente disponíveis, que não foram desenvolvidos especificamente para uso médico. Eles foram selecionados por causa da combinação desejável de propriedades físicas específicas, para o uso clínico pretendido, e porque, eram bioinertes, ou seja, eles provocavam uma resposta mínima a partir dos tecidos do hospedeiro, portanto, eles foram considerados biocompatíveis.
O carbono pirolítico, originalmente desenvolvido na década de 1960 como um material de revestimento para partículas de combustível nuclear, é agora amplamente utilizado em composições modificadas para componentes de revestimento de válvulas cardíacas mecânicas.
A segunda geração de biomateriais evoluiu dos primeiros biomateriais, e destina-se a
provocar uma reação controlada com os tecidos nos quais foram implantados, a fim de induzir um efeito terapêutico desejado. Na década de 1980, esses materiais bioativos foram utilizados
clinicamente em cirurgias dentais e ortopédicas. Dentre os principais exemplos dessa geração estão os biovidros e as biocerâmicas utilizados em ortopedia, válvulas cardíacas, dispositivos de assistência ventricular e stents (utilizados em procedimentos de cateterismos). A segunda geração de biomateriais ainda incluía o desenvolvimento de biomateriais reabsorvíveis, com taxas de degradação adaptadas aos requisitos de uma aplicação pretendida. Assim, a interface discreta, entre o local do implante e o tecido hospedeiro pode ser eliminada em longo prazo, porque o material estranho seria, em última análise, degradado como é o caso das suturas composta por ácido poliglicólico-PLA, usada desde os anos 60. Muitos grupos continuam pesquisando polímeros biodegradáveis que precisam de propriedades tais como, resistência, flexibilidade, uma composição química condutora para o desenvolvimento do tecido, e uma taxa de degradação de acordo com a aplicação específica. Materiais poliméricos com outras propriedades novas como memória de forma e superfícies programáveis e interativas, que controlam o microambiente, celular ainda estão em investigação.
A terceira geração de biomateriais, a extensão lógica do estado da arte, vem progredindo
rapidamente e tem o objetivo de apoiar e estimular a regeneração do tecido funcional. Ao longo de toda a história humana, a habilidade médica para realmente regenerar tecidos e órgãos perdidos, devido a uma doença ou trauma, era essencialmente inexistente; o papel do médico, no passado, estava aliado a medidas paliativas (aliviar os sintomas sem curar). Atualmente, com os avanços nas ciências, engenharia de tecidos e da medicina regenerativa, parece que a verdadeira substituição por tecido vivo será possível. Biomateriais irão desempenhar um papel-chave no desenvolvimento da engenharia de tecidos e na terapêutica regenerativa.
A engenharia de tecidos é um termo amplo que descreve um conjunto de ferramentas na
interface das ciências biomédicas e engenharia, que utilizam células vivas (ou atrair células
endógenas) para auxiliar a formação ou regeneração de um tecido. No paradigma mais
frequentemente utilizado, as células são semeadas num scaffold composto de polímero sintético ou material natural, um tecido é maturado in vitro, e a construção é implantada na localização anatômica apropriada, como uma prótese. Um scaffold típico pode ser um material em uma configuração porosa, com a geometria desejada para a engenharia de tecidos, frequentemente modificada para aderir às células.
Dessa maneira, a engenharia de tecidos levou à substituição de bexiga, traqueia, pele, epitélio da córnea e cartilagem danificados. As direções futuras em biomateriais, engenharia de tecidos e terapias regenerativas, são realmente motivadoras e estão em discussão ativa.
Hidroxiapatita
A hidroxiapatita sintética é um dos materiais bioativos mais utilizados como enxerto ósseo, pois permite a formação de ligações químicas com a hidroxiapatita óssea, promovendo a osseointegração. Essas ligações são de natureza covalente e isso faz com que a interface entre o tecido vivo e o implante suporte esforços mecânicos significativos.
Quando obedecida a estequiometria, a hidroxiapatita apresenta uma razão molar Ca/P de 1,67. Este valor foi obtido por meio das técnicas de difração de raios-X e difração de nêutrons. No caso das hidroxiapatitas deficientes em cálcio o valor da razão Ca/P pode variar em 10%.
A hidroxiapatita possui estrutura cristalina hexagonal com grupo espacial P63/m (176) caracterizado por uma simetria perpendicular aos três eixos “a” equivalentes (a1, a2 e a3), formando um ângulo de 120º entre si. Os parâmetros de rede da cela unitária, para a hidroxiapatita estequiométrica correspondem a: a = b= 0,9432 nm e c = 0, 6881 nm.
Na hidroxiapatita, os átomos de fósforo aparecem sempre cercados por quatro átomos de oxigênio situados nos vértices de um tetraedro (Figura 2). Dessa maneira, a hidroxiapatita consiste de um esqueleto de tetraedros do grupo (PO43-) com dois átomos de oxigênio no plano basal e outros dois alinhados com o eixo cristalográfico “c”. Na Figura 2 a célula unitária da hidroxiapatita é ilustrada. As esferas amarelas, azuis, fúcsias e vermelhas representam os átomos de cálcio, fósforo, oxigênio e hidrogênio, respectivamente.
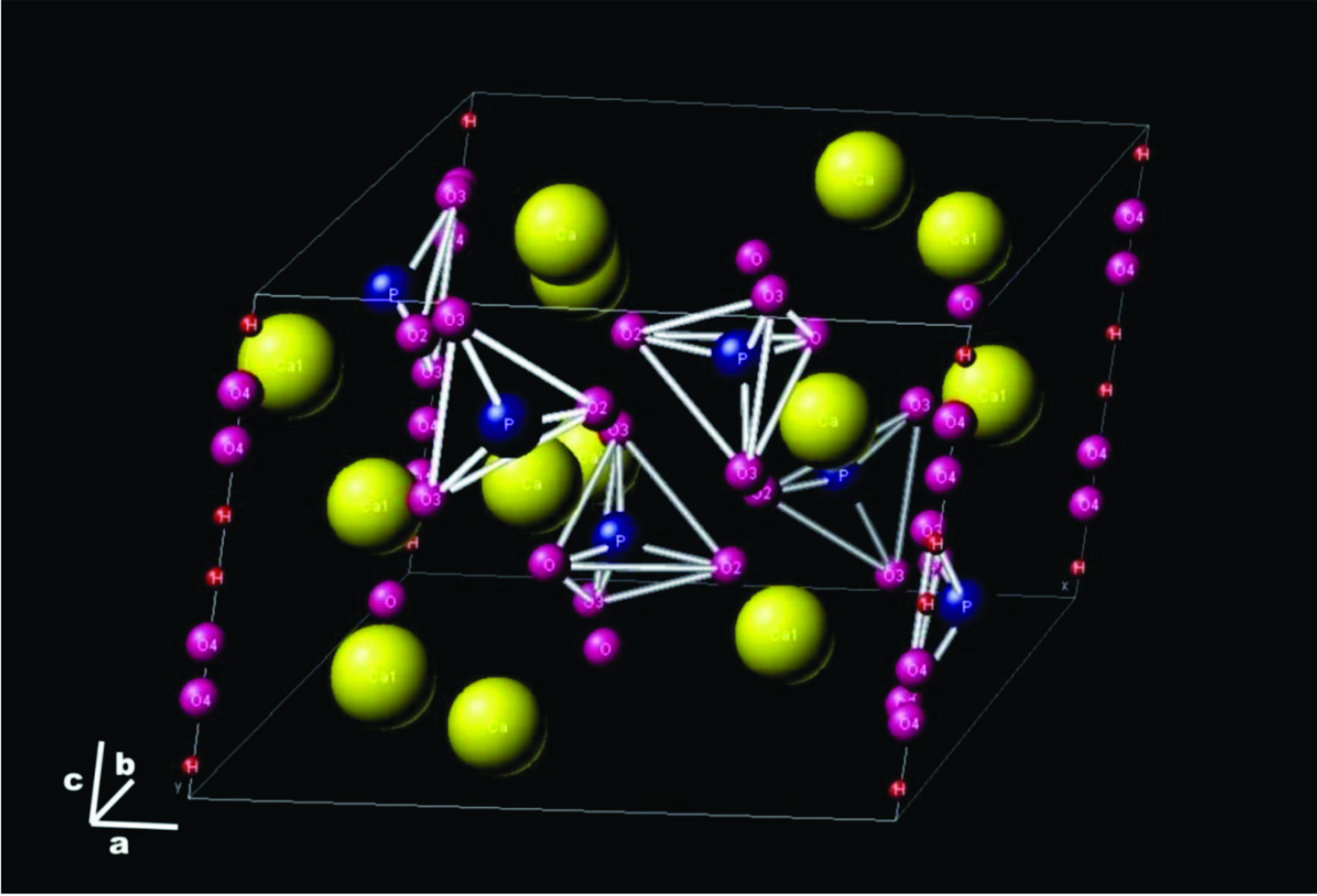
Figura 4: Representação esquemática da estrutura cristalina (cela unitária) da hidroxiapatita.
Eventualmente podem ocorrer substituições de sítios no interior da estrutura cristalina. No caso da hidroxiapatita, os elementos Ca2+, PO43- e OH- são substituídos por outros íons com cargas de mesmo sinal. É o caso, por exemplo, do grupo carbonato CO32- que pode tanto ocupar a posição estrutural do OH- (substituição do tipo A) como ocupar a posição do íon PO43- (substituição do tipo B) . O íon carbonato é capaz de causar uma tensão na rede cristalina da HA fazendo com que a taxa de dissolução do material aumente. Isso ocorre inclusive nos ossos que, por sua vez, têm muitos elementos substituídos em sua estrutura cristalina.
Os cátions K+ e Na+ são capazes de substituir o íons Ca2+ sem alterar os parâmetros de rede da HA, no entanto a substituição que ocorre quando o Ca2+ é substituído pelo Mg2+ é capaz tanto de alterar parâmetros de rede da estrutura cristalina quanto diminuir a cristalinidade do material. Substituições de OH- por Cl- comumente alteram parâmetros de rede sem alterar a cristalinidade. As substituições do tipo B do carbonato alteram os parâmetros de rede e a cristalinidade e a substituição por HPO42- não alteram a cristalinidade, mas aumenta o parâmetro de rede “a”.
Vários métodos são utilizados para sintetizar hidroxiapatita. Uma das primeiras técnicas para produzir HA foi a exposição hidrotérmica da fluorapatita (Ca10(PO4)6F2) a altas temperaturas e pressões (Levitt e colaboradores). Os métodos mais utilizados são por via úmida e via seca, mecanosíntese, hidrotermal, sono químico, sol-gel, entre outros.
Um método que se destaca por sua facilidade é a calcinação de ossos “in natura”. O método desenvolvido por Lima e Weinand, possibilita obter hidroxiapatita natural e de boa qualidade a partir de osso de peixe. Assim, é possível produzir um material natural cuja matéria prima se encontra disponível em qualquer região do país. Outra vantagem desse procedimento é seu baixo custo não só pelo fato de utilizar ossos de peixe (que não têm valor comercial expressivo), como também porque as temperaturas de calcinação empregadas são relativamente baixas (em torno de 900 °C).
β – fosfato tricalcio
O β – fosfato tricálcico é um material que pode ser facilamente reabsorvido pelo corpo animal. Além disso, por ser bioativo, atóxico, osteocondutor e biodegradável, não há a necessidade de uma segunda operação cirúrgica para remover o dispositivo implantado, após a cura se processar.
A cerâmica Ca3(PO4)2 possui razão Ca/P de 1,5 e pertence ao grupo espacial R3c de simetria hexagonal com cela unitária a = b = 1,0439 nm e c= 3,7375 nm. Para cada cela unitária hexagonal, há 21 formulas unitárias e 42 tetraedros (PO43-). A cela unitária da fase β-TCP está representada na Figura 3. As esferas em verde, laranja e vermelho representam os átomos de cálcio, fósforo e oxigênio, respectivamente.
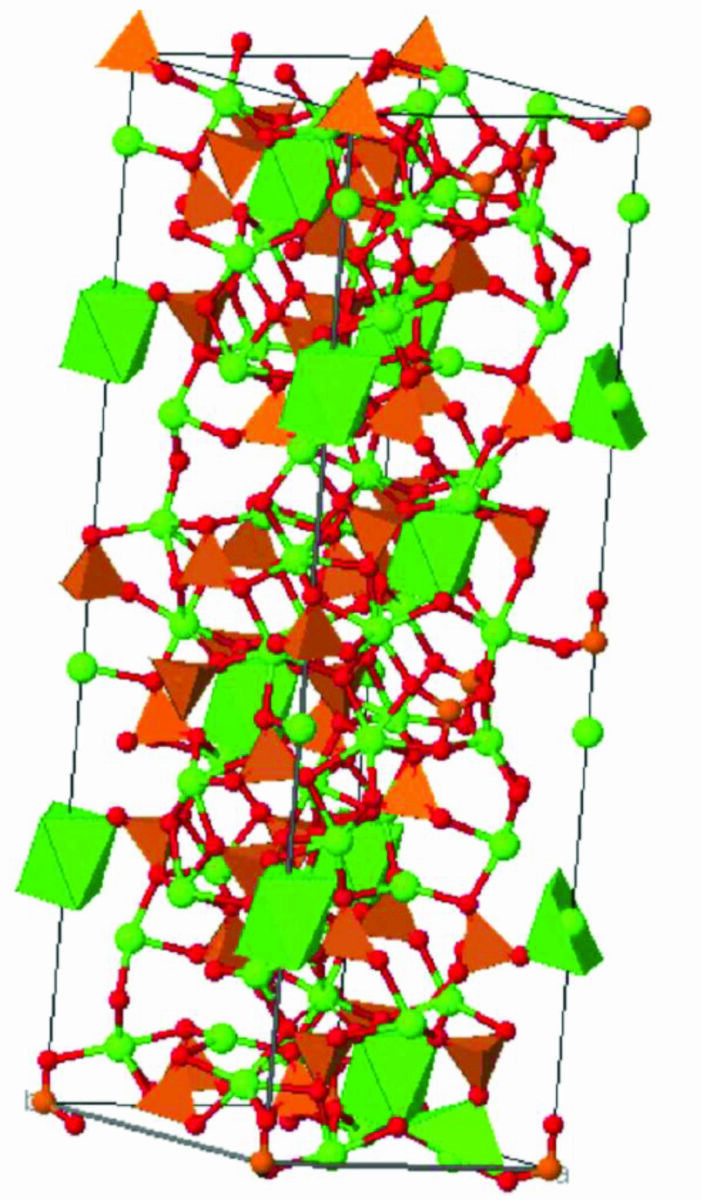
Figura 3: Representação esquemática da estrutura cristalina da fase β-TCP, adaptada da referência.
O β-TCP permite a substituição de 15% dos átomos de Ca2+ por Mg2+ sem alterar ssencialmente sua estrutura. Quando o magnésio Mg2+ está presente na estrutura, o material apresenta enor solubilidade. Se o Mg2+ ocupar a posição Ca (5), a estabilidade da rede aumenta, pois a substituição é de um cátion maior (raio iônico = 0,99Å) por um menor (raio iônico =0,65 Å), no caso o Mg2+.
Referencias
http://www.pfi.uem.br/wp-content/uploads/2015/11/taiana_gabriela_moretti_bonadio_2014.pdf
















